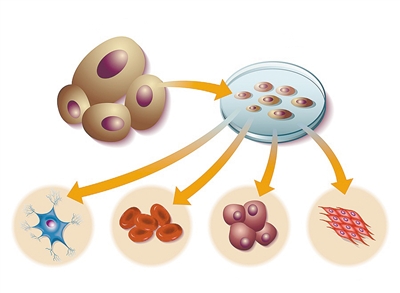
诱导多能干细胞具有早期胚胎干细胞的发育能力,理论上可以分化成任何类型的成体细胞和器官。
东京医科牙科大学最近宣布,其研究人员与美国同行合作,利用人类诱导的多能干细胞生产三种微型器官:肝脏、胆管和胰腺。
自古以来,永生就是无数人的梦想。现在,一群科学家正在延长人类寿命和提高健康质量的前线战斗。
最近,器官培养研究取得了新的突破。迄今为止,诱导多能干细胞(iPS cells)只能用于培养特定的细胞和器官。然而,东京医科牙科大学最近宣布,其研究人员与美国同行合作,利用人类诱导多能干细胞同时培养三种微型器官:肝脏、胆管和胰腺。研究结果已经发表在《自然》杂志的网络版上。
利用诱导多能干细胞培养人体器官的主要原则是什么?与单独培养一个器官相比,用iPS细胞同时培养多个器官有什么困难?这些器官再生技术何时真正达到临床阶段?可能的挑战是什么?有了这些问题,《科学技术日报》的记者采访了该领域的相关研究人员。
没有伦理问题困扰诱导多能干细胞成为“热蛋糕”
“诱导多能干细胞有能力发展早期胚胎干细胞。体外培养,诱导多能干细胞理论上可以通过构建合适的环境,如添加生长因子、设计生长基质等,分化成任何类型的成体细胞和器官。以模拟体内发育过程。”中国科学院广州生物医学与健康研究所研究员陈洁凯在接受《科技日报》采访时说。
"如果一个器官被视为一棵树,iPS细胞就像种子。浇水和施肥后,诱导多能干细胞分化为器官的不同细胞类型,就像树叶、树干和树枝一样。”该研究所的研究员刘晶解释了用iPS细胞以流行的方式培养器官的原理。
iPS细胞实际上是干细胞家族中的“长者”,从它的名字可以看出。“多能性”表明这种干细胞具有巨大的分化潜力,而“诱导性”表明人类因素参与了其获取过程。
与直接从胚胎获得的干细胞不同,诱导多能干细胞是由体细胞诱导的,即首先获得体细胞,然后在体外实验条件下引入特异性转录因子,将体细胞“重新编程”为诱导多能干细胞。这种诱导过程就像一种神奇的魔法,它能使人体分化链末端的体细胞“再生”,并恢复类似胚胎干细胞的发育潜能,逆转生命的时钟。
科学家如果想获得iPS细胞,理论上可以使用人体内所有类型的体细胞作为“原料”。然而,胚胎干细胞通常只能从早期胚胎或原始性腺中分离出来。相比之下,诱导多能干细胞来源广泛,具有很大优势。当然,简化诱导程序和提高诱导效率以及其他相关问题也是科学家目前面临的挑战。"利用患者自身或免疫匹配的诱导多能干细胞进行器官培养可以有效减少临床移植中的排斥反应."刘晶说,传统的器官移植通常是同种异体移植,患者应该在手术后长时间服用免疫抑制药物,以减少或消除排斥反应。IPS细胞可以改变这种情况,有助于术后恢复。
更重要的是,“诱导多能干细胞是在不使用胚胎细胞或卵细胞的情况下产生的,因此不存在伦理问题。”刘晶说。
事实上,胚胎干细胞研究在一些国家是一个有争议的领域。反对者认为胚胎干细胞研究必须摧毁胚胎,胚胎是人类形成前子宫中的生命形式,这违背了生物伦理。IPS细胞不再受伦理问题的困扰。自2006年日本科学家山中伸弥(shinya yamanaka)提出以来,一直非常受欢迎,成为相关领域的“热门话题”。
陈洁凯告诉记者,近年来科学家们已经将其应用于小“微型”器官的研究,这种器官在学术界通常被称为“类器官”。顾名思义,类似的器官在某种程度上类似于特定的器官。目前,初级商品特别股
陈洁凯指出,与单个器官相比,同时诱导多个器官的困难在于两点:不同器官发育信号条件不同,如何同时模拟;不同器官的发育需要iPS细胞分化成不同种类的起始细胞,以及如何获得合适的起始细胞并以合适的比例混合它们。
虽然器官培养的数量只有1和N的差异,但困难远非简单的1 1=2的叠加。“当培养多个器官时,需要考虑的影响因素变得更加复杂,培养条件也变得更加复杂。更重要的是,不清楚培养的多器官之间是否有任何协同作用,以及有什么样的协同作用。”刘晶说。
大多数时候,高难度意味着高回报。陈洁凯认为,如果多器官由iPS细胞培养,器官之间有很强的协同作用,那么多器官合作培养将更好地模拟体内的环境。此外,在药物筛选过程中,多器官培养也可以及时排除对其他器官有副作用的候选药物。
刘晶还说多器官共同培养可能会导致功能更好、更接近真实器官的“人造”器官。此外,随着技术的发展,合作文化的效率可能会高于单一文化。
这次,日本研究人员培育了三种器官:肝脏、胆管和胰腺。这是偶然的还是不可避免的?肝、胆管和胰腺都来源于胚胎的内胚层,三者发育相似刘晶说。鉴于iPS细胞的单器官培养仅处于相对早期的研究阶段,更不用说多器官再生领域。因此,研究人员自然会首先关注相对简单的模型。“我相信许多研究者也在研究胚胎中胚层和外胚层的多器官再生。”刘晶说。
目前只移植组织和器官远非临床。
当提到iPS细胞和移植时,我相信很多人会想到不久前相对轰动的角膜移植。
今年8月底,日本大阪大学的一个研究小组完成了世界上第一次移植用诱导多能干细胞培养的角膜组织的临床手术。这是否意味着iPS细胞器官移植的临床应用即将到来?
在刘晶看来,角膜是一种不同于器官的组织。器官培养更困难,但在现有研究的基础上移植组织是很好的
陈洁凯也认为器官样技术离临床实践还很远。目前,作为器官发育的体外模型,它可用于研究疾病病理学和进行药物筛选。
利用iPS细胞培养与真实器官具有相同结构、体积和功能的人工器官还有很多工作要做,在此期间还有很多挑战。
"血管形成、大小等。可能是需要解决的相对较好的技术问题。真正的瓶颈在于体内功能和移植方法。”陈洁凯说。
刘晶说器官功能的研究难点包括空间维度和时间维度。例如,从平面上的2D到立体上的3D,空间复杂度增加;例如,当研究人员突破类器官的范畴,培养出接近真实体积的器官时,系统的增加会导致一些反馈相对较慢,时间复杂度也会增加。"此外,动物模型的选择和相关药物的筛选也是有待解决的问题."
“目前,世界上有许多研究人员正在努力克服这一领域的困难。科学有任何可能性。也许再过5-10年,由诱导多能干细胞培养的器官可以在一定规模上应用于临床。”刘晶说。